Petz Aladár Megyei Kórház, IV. Belgyógyászati osztály,1 Györ; fővárosi Bajcsy-Zsilinszky Kórház, III.
Belgyógyászati osztály,2
Budapest
NIDDM-ES BETEGEK MIKRONIZÁLT
GLIBENCLAMID (GLUCOBENE®) KEZELÉSE SORÁN SZERZETT KLINIKAI
TAPASZTALATOK
Hidvégi Tibor dr.,1 Jermendy György dr.2
Összefoglalás
A szerzők nyílt klinikai vizsgálat
kapcsán, újonnan felismert NIDDM-es betegek körében (életkor [x±SD]: 51,9±8,2 év,
n=30) diétás kezelés elégtelenségét követően mikronizált glibenclamid (Glucobene®) terápiát kezdtek, a kezdő dózis az esetek
jelentős részében 1,75 mg volt. A három hónapra terjedő megfigyelés során az
alapvizsgálati helyzethez viszonyított laboratóriumi paraméterek a szénhidrát
anyagcsere helyzetének számottevő javulását tükrözték (éhgyomri vércukor:
12,2±2,7 mmol/l vs 8,2±1,9 mmol/l, p<0,001; cukorürítés: 129±210 mmol/nap vs
7±22 mmol/nap, p<0,01; HbA: 8,6±1,3% vs 6,6±0,8%, p<0,001). Adverz esemény nem
fordult elő, hypoglykaemiás epizódról a betegek nem számoltak be. Az előnyös
felszívódási tulajdonságokkal rendelkező mikronizált glibenclamid (Glucobene) jól
használható NIDDM-es betegek kezelésekor, ha a diétás elöírások önmagában nem
elégségesek a megfelelő anyagcsere-egyensúly biztosításához.
Kulcsszavak: NIDDM-es
betegek, sulfonylurea, mikronizált glibenclamid
Clinical experiences with micronized
glibenclamide (Glucobene®) for treating NIDDM-patients
Summary
To get clinical experiences, treatment
with micronized glibenclamide (Glucobene®) was initiated in 30 NIDDM-patients
(age: 51.9±8.2 years, x±SD) when dietary restrictions have failed. The initial dose of
the drug was 1.75 mg in most cases. Significant improvement could be detected by
laboratory parameters by the end of the 3-month-long investigation period (fasting blood
glucose 12.2±2.7 mmol/l vs 8.2±1.9 mmol/l, p<0.001; urinary glucose excretion
129±210 mmol/die vs 7±22 mmol/die, p<0.01; HbA1c 8.6±1.3 % vs 6.6±0.8 %,
p<0.001). Neither adverse events nor hypoglycaemic episodes were recorded during the
open clinical study. Micronized glibenclamide (Glucobene®) with its beneficial intestinal
absorption proved to be useful for treating NIDDMpatients when dietary restrictions have
failed.
Key words: NIDDM-patients,
sulphonylureas, micronized glibenclamide
Jól tudott, hogy újonnan felismert NIDDM-es betegek kezelése diétás és
életmódbeli rendszabályok elöírásával kezdödik. A betegek egy részében azonban a
diéta önmagában nem elégséges, s orális antidiabetikus kezelés bevezetése válik
szükségessé. Az orális antidiabetikumok legrégebbi hatástani csoportjába a
sulfanylurea-származékok tartoznak. E csoporton belül a glibenclamid
vércukorcsökkentő hatása nemcsak kifejezett, hanem tartós is. A glibenclamid ma
hazánkban a legszélesebb körben alkalmazott orális antidiabetikum, de örvendetes
módon az újabb sulfanylurea-származékok piacra kerülésével egyre inkább
lehetőség nyílik a NIDDM-es betegek differenciált terápiájára is.1
A glibenclamid jobb biológiai hasznosulásának érdekében micronizált
készítményt állítottak elő, amelyet a Ludwig Merckle cég Glucobene® néven, 1,75 mg-os és 3,5 mg-os
kiszerelésben a közelmúltban hozott forgalomba Magyarországon.
Hazai tapasztalatszerzés érdekében, nyílt klinikai vizsgálat kapcsán,
újonnan felismert NIDDMes betegek körében, diétás kezelés elégtelenségét
követően Glucobene®-terápiát kezdtünk. Jelen
dolgozatban a klinikai megfigyelés tapasztalatait összegezzük.
Betegek és módszerek
Belgyógyászati osztályon, ill. diabetológiai járóbetegrendelésen
jelentkező, újonnan felismert NIDDM-es betegeket vizsgáltunk. A 2. típusú diabetes
mellitus kórisméje klinikai ismérveken alapult. Tanulmányunk nyílt klinikai
vizsgálat volt. A beválasztási kritériumok az alábbiak voltak: életkor 35–70 év
között, 3 hónapra terjedő, adekvát diétás kezelés eredménytelensége, szérum
creatinin <150 µmol/l. A csak diétás kezelés eredményeképpen az éhgyomri
vércukor és a test-tömeg index szignifikánsan (13,0±2,7 mmol/l vs 12,2±2,7 mmol/l,
p<0,001; ill. 30,2±4,8 kg/m2 vs 30,0±4,7 kg/m2, p<0,001), a cukorürítés
tendenciaszerüen (136±191 mmol/nap vs 129±210 mmol/nap p>0,05) csökkent, de orális
antidiabetikus kezelés mellett döntöttünk, ha az éhgyomri vércukor >8,0 mmol/l
maradt. Így a gyógyszeres kezelési periódus alapvizsgálati időpontjában a >8,0
mmol/l vércukor beválasztási kritériumnak minösült. Nem vontunk be a tanulmányba
terhes vagy szoptató nöt, alkoholt rendszeresen fogyasztót, májbetegségben
szenvedöt, ill. olyan beteget, akinek elözményi adatai között a gyomor-bélhuzam
betegsége szerepelt. A heveny anyagcserezavar (acetonuria) szintén kizáró ok volt. A
betegek a tanulmányban való részvételhez hozzájárulásukat adták.
A 3 hónapra terjedő gyógyszeres kezelési periódus során az alábbi
paramétereket vizsgáltuk: test-tömeg index, éhgyomri vércukor, cukorürítés, HbA1c, szérum cholesterin, triglycerid,
HDL-cholesterin, creatinin. Rögzítettük az esetleges nemkívánatos mellékhatásokat,
ill. a hypoglykaemiás epizódok számát.
Hypoglykaemiát állapítottunk meg, ha rosszullét kapcsán a beteg vércukra
dokumentáltan <3,0 mmol/l volt. Az alapvizsgálat után a betegeket havonta,
járóbetegként ellenőriztük. A HbA1c értékét csak a gyógyszeres
kezelési periódus kezdetén és végén határoztuk meg.
A vércukor, a szérum lipidek és a kreatinin meghatározása standard
laboratóriumi módszerekkel, éhgyomri vérmintából történt. A cukorürítést 24
órás gyűjtött vizeletmintát használva állapítottuk meg. A HbA1c értékét HPLC-módszerrel határoztuk
meg (normális tartomány 4,0%–6,0%). Jó anyagcserehelyzetnek értékeltük, ha a HbA1c értéke <7,5% volt.
Vizsgálatunkban 30 NIDDM-es beteg szerepelt, a betegcsoport fontosabb jellemzői a
gyógyszeres kezelési periódus alapvizsgálati időpontjában az alábbiak voltak: 15
férfi, 15 nő, életkor 51,9±8,2 év, test-tömeg index 30,0±4,7 kg/m2, szérum kreatinin 87±17 µmol/l,
éhgyomri vércukor 12,2±2,7 mmol/l, cukorürítés 129±210 mmol/die, HbA1c 8,6±1,3% (x±SD).
A klinikai körülményeket figyelembe véve arra törekedtünk, hogy a Glucubene® kezdő dózisa 1,75 mg (reggel,
étkezés előtt) legyen. Az aktuális vér- és vizeletcukor értéke, ill. a testsúly
alapján a kezdő dózis egyénileg megállapítva magasabb, de maximum 5,25 mg/nap
(reggel 3,5 mg, délben 1,75 mg) is lehetett. A havonkénti ellenőrzés során a
Glucubene® dózisát az összes körülmény
(aktuális vércukor és cukorürítés, ill. az előző vizsgálati eredményhez
viszonyított változás mértéke) figyelembevételével, egyéni mérlegelés alapján
növeltük. Nagyobb dózis szükségessége esetén a három föétkezés előtt adtuk a
gyógyszert, törekedve arra, hogy napi eloszlásban a legkisebb dózis az esti legyen. A
gyógyszer maximális dózisának a 14,0 mg-t tekintettük. A tanulmányt a harmadik
hónap végén zártuk, de a betegek továbbra is gondozásunk alatt maradtak.
Az adatok statisztikai értékelése során a Student-féle egymintás t-próbát
használtuk. A p<0,05 értéket tekintettük szignifikáns eltérésnek. A dolgozatban
az átlag és a standard deviatio (x±SD) értékét tüntettük fel.
Eredmények
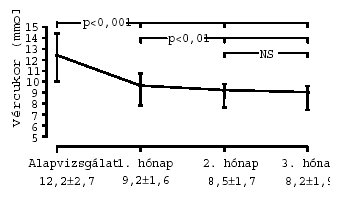
A Glucobene már 1 hónapos alkalmazást követően szignifikáns módon
csökkentette az éhgyomri vércukorértéket, s a későbbiekben is megfigyelhető volt
további – mérsékeltebb fokú – vércukorcsökkentő hatás (1. ábra). A Glucobene® alkalmazásának kezdetén minden
beteg éhgyomri vércukorértéke – a beválasztási kritériumból adódóan –
>8,0 mmol/l volt, a tanulmány végén 19 beteg esetében találtunk =8,0 mmol/l
vércukorértéket.
A cukorürítés mértéke a megfigyelés során fokozatosan, statisztikailag
értékelhető módon csökkent (2. ábra). A tanulmány zárásakor 24 beteg
aglycosuriás volt.
A Glucobene®-kezelés során a HbA1c-érték számottevően csökkent
(3. ábra). A Glucobene® alkalmazásának kezdetekor 24 beteg
esetében, a záráskor viszont csak 4 beteg vizsgálata során találtunk >7,5% HbA1c-értéket (utóbbi egyedi értékek:
7,6%; 7,8%; 7,9%; 8,2%).

1. ábra: Az éhgyomri vércukorérték alakulása cukorbetegek Glucobene®-kezelése során (n=30i; x±SD)
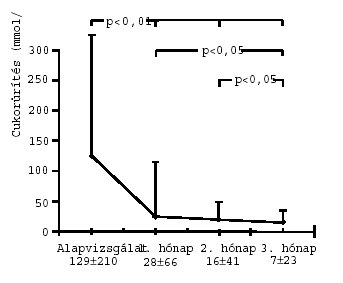
2. ábra: A cukorürítés alakulása cukorbetegek Glucobene®-kezelése során (n=30; x±SD)
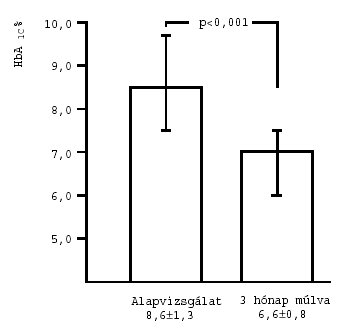
3. ábra: A HbA1c-érték alakulása cukorbetegek Glucobene®-kezelése során (n=30; x±SD)
A Glucobene®-kezeléssel elért jobb
szénhidrátanyagcsere-helyzet a szérum lipidek (összcholesterin, triglycerid) előnyös
alakulását vonta maga után (1. táblázat).
A betegek jelentős hányadában kezdő dózisként elégséges volt az 1,75 mg
kiszerelésű Glucobene ®
adása, később
azonban a dózist a betegek egy részében növelni kellett (2. táblázat). A tanulmány
során a betegek testtömeg-indexe (3. hónapban 30,0±3,9 kg/m2) és szérum kreatinin értéke (3.
hónapban 88±18 µmol/l) érdemben nem változott.
A Glucobene®-kezelés során adverz eseményt
nem észleltünk, a betegek hypoglykaemiás epizódról nem számoltak be.
| Alapvizsgálat | 1. hónap | 2. hónap | 3. hónap | |
| Szérum cholesterin (mmol/l) |
6,55±1,81 | 6,10±1,25* | 5,81±0,97+** | 5,68±0,98++** |
| Szérum triglycerid (mmol/l) |
4,67±4,44 | 3,15±2,20** | 3,08±2,35* | 2,71±1,72** |
| Szérum HDL-cholesterin (mmol/l) |
1,12±0,48 | 1,10±0,30 | 1,11±0,24 | 1,17±0,30 |
* p < 0,05 az alapvizsgálati értékhez viszonyítva |
||||
| Glucobene® napi dózisa |
Betegek száma a megfigyelés | |
| mg | kezdetén | végén |
| 1,75 | 17 | 9 |
| 3,50 | 5 | 6 |
| 5,25 | 8 | 7 |
| 7,00 | 0 | 4 |
| 10,50 | 0 | 3 |
| 14,00 | 0 | 1 |
2. táblázat: A betegek megoszlása a Glucobene® dózisa szerint
Megbeszélés
Nyílt klinikai vizsgálatunk során kedvező tapasztalatok szereztünk
micronizált glibenclamid adásával NIDDM-es betegek körében: a három hónapra
terjedő megfigyelés során a szénhidrátanyagcsere jelentős javulását figyelhettük
meg.
Adverz eseményt, hypoglykaemiát a vizsgált betegcsoportban nem észleltünk.
A sulfanylureák a legrégebben ismert és a legszélesebb körben használt
orális antidiabetikumok.
Az évek folyamán az első generációs készítményeket felváltották a
második generációhoz sorolt vegyületek, ma lényegében csak az utóbbiak
használatosak. A hazai választék az utóbbi években egyre bövült, így a korábbi
– meglehetösen uniformizált – sulfanylurea-kezelés helyett ma már lehetőség van
e téren differenciált terápiát folytatni, azaz a készítmény megválasztásakor
mérlegelhetjük az egyes készítmények sajátos előnyét, s tekintettel lehetünk az
adott beteg tényleges klinikai állapotára (napszaki vércukorértékek, veseműködés
stb.) is.1 NIDDM-es betegek
sulfanylurea-kezelését akkor célszerű indikálni, ha a hosszabb ideig tartó diétás
kezelés és életmódbeli elöírások (sok mozgás, sportolás) nem hoznak kellö
eredményt, s a beteg normális testsúlyú vagy legalábbis jelentős
testsúlyfelesleggel nem rendelkezik.2 Az elhízott cukorbetegek elsö
orális antidiabetikumaként helyesebb biguanidkészítményt vagy
alfa-glukozidáz-gátló szert választani.3,4 Bár az elvet igyekeztünk követni,
tanulmányunk időpontjában (1997-ben) a gyakorlati hozzáférhetöség korlátokat
szabott az elv érvényesítésének.
E körülményt tekintve kell értékelni betegcsoportunk átlagos
testtömeg-indexét. Gondunk általános hazai jelenségre utal,4 s csak örülni lehet, hogy
napjainkban megtörtént a metformin regisztrációja és az acarbose forgalmazása végre
támogatásban részesül, biztosítva, hogy a jövöben az orális antidiabetikus
kezelés gyakorlata hazánkban egyre közelebb kerülhet majd az elvekhez.
A sulfanylureák között a glibenclamid a leggyakrabban rendelt szer, ezt a
felhasználási jellegzetességet nemcsak hazánkban, hanem számos más országban is meg
lehet figyelni.4 A glibenclamid anyagcserehatása
eröteljes, hatástartama hosszú, metabolitjainak egy része is aktív, így a
kumuláció lehetősége – különösen beszűkült vesefunkció esetén – a
hypoglykaemia veszélyét rejti magában.3 A glibenclamid előnye a kedvezö
antiarrhythmiás hatás,5,6
ami nem lebecsülendö
körülmény a coronaria-betegség várható gyakorisága miatt. A glibenclamid
előzőekben említett tulajdonságai miatt adása magas életkorban kerülendő, s a
vesefunkció romlása szintén a szer alkalmazásának kontraindikációját jelenti. E
körülményekre betegeink beválasztásakor tekintettel voltunk.
A glibenclamid-kezelés mellett kialakuló hypoglykaemia az irodalomban jól
dokumentált, 7,8 a mindennapos gyakorlatban azonban
talán kevésbé közismert, hogy ilyen körülmények között a hypoglykaemia gyakran az
éjszakai órákban, agyi inzultus képében jelentkezik.9 A hypoglykaemia lehetősége
elötérbe helyezi az adekvát dózis (s a helyes indikáció) kérdését, noha nem
vitás, hogy az esetek egy részében a nemkívánatos mértékű vércukorcsökkenés a
beteg hibájából eredöen (étkezés elhagyása, alkoholfogyasztás következtében)
alakul ki. Tanulmányunk során hypoglykaemiás epizódot nem regisztráltunk. Fontos
adat, hogy hazai megfigyelés szerint mikronizált glibenclamid mellett a hajnali (03
órakor mért) vércukor magasabb volt, mint ugyanezen betegek hasonló értéke
nem-mikronizált glibenclamid kezelése mellett.10
A hagyományos glibenclamid hazánkban elérhető legkisebb kiszerelése a
tablettánkénti 5,0 mg, talán érdemes lenne figyelembe venni, hogy a nemzetközi
irodalomban is vannak kedvező tapasztalatok a hagyományos glibenclamid alacsonyabb
dózisú kezelésével.11
A Glucobene® elönye, hogy 1,75 mg-os
kiszerelése alacsony kezdő dózis lehetőségét biztosítja, amit a betegeink jelentős
hányadában ki is tudtunk használni.
A glibenclamid mikronizált formája jobb, gyorsabb, megbízhatóbb (kevésbé
variábilis) felszívódást és tökéletesebb biológiai hasznosulást biztosít.12,13 E körülménynek nagy a
jelentősége, mert cukorbetegekben a felszívódás bizonytalan volta értelemszerüen
nehezíti a jó anyagcsereegyensúly elérését. Igazolták, hogy cukorbetegekben a
hyperglykaemia lassítja a glibenclamid felszívódását. 14 A gyomor-bélrendszert érintö
autonom neuropathia jelenléte szintén elhúzódóvá teszi a gyógyszer
felszívódását.15 E körülményekre tekintettel
nyilvánvalóan előnyös a megbízható felszívódást biztosító mikronizált
kiszerelési forma használata. A mikronizált előállítási forma jobb biológiai
hasznosulását jelzi, hogy kisebb dózissal érhető el a hagyományos glibenclamid
adásakor megfigyelhető, azonos mértékű és jellegű béta-sejt (inzulin, C-peptid)
-válasz.12,16 Ez azt jelenti, hogy a 3,5 mg-os
kiszerelésű mikronizált glibenclamid biológiailag ekvivalensnek tekinthető 5,0 mg
hagyományos glibenclamiddal.17 E ténnyel függhet össze, hogy a
mikronizált és a hagyományos glibenclamid felszívódásában megmutatkozó
különbség ellenére az anyagcsere-hatás, azaz a vércukorértékek alakulása (a
biológiai ekvivalensnek tekintett mennyiségek esetén) érdemben nem különbözött
egymástól.18 Ezzel szemben egy másik vizsgálatban
azt tapasztalták, hogy micronizált glibenclamid alkalmazásakor, rövidebb távon, a
postprandialis vércukor és a HbA1c értéke szignifikánsan alacsonyabb
volt, mint a hagyományos glibenclamid mellett észlelt érték.13 Más szerzők mikronizált
glibenclamid mellett jobb vércukorprofilt észleltek, mint hagyományos glibenclamid
alkalmazásakor.16 E téren az adatok ellentmondóak,18 ezért hosszú távú megfigyelések
szükségesek még, s csak azok eredményét tekinthetjük majd mérvadónak.
A NIDDM-es betegek orális antidiabetikus kezelése csak látszólag jelent
egyszerű orvosi feladatot. A diabetes klasszifikációja (és a diabetestípusnak
megfelelő kezelés megválasztása) az esetek egy részében gondot jelent.19 Ha a diabetes típusa nem kétséges,
s ténylegesen NIDDM-röl van szó, a megfelelő terápiával elért korrekt
anyagcserevezetés a késői szövődmények elkerülése érdekében nagy jelentőségű.
A UKPDS tanulmány végső analízisétöl sok új információt remélünk e téren, de a
jelenleg rendelkezésre álló adatok szerint úgy látszik, hogy a NIDDM-es betegek egy
hányada – a terápiás törekvések ellenére – mégiscsak hyperglykaemiás marad.20 Magunk is a tanulmány zárásakor –
a Glucobene® kedvező anyagcserehatása ellenére
– néhány beteg esetében még további terápiás eröfeszítésre ösztönzö
éhgyomri vércukorértéket tapasztaltunk. Általánosságban véve nem vitás, hogy
NIDDM-es betegek orális antidiabetikus kezelésével kapcsolatban még több, nyitott
kérdésre kell a kutatásnak és a klinikai megfigyeléseknek a jövöben választ
adniuk.
IRODALOM
1. Winkler G, Simon K, Tóth J, Gyulai
M: Szemléletváltozás a 2. (nem inzulindependens) típusú cukorbetegség kezelésében.
Orv Hetil 138: 1043-1051, 1997.
2. Pogátsa G: Orális
antidiabeticumok. A cukorbetegség klinikai vonatkozásai (in: Halmos T, Jermendy Gy,
(szerk.): Diabetes mellitus, Medicina, Budapest, 1997. pp. 215-230.
3. Tamás Gy, Kerényi Zs: Az orális
antidiabetikumok helye a diabetes mellitus kezelésében. Kórház 2 (7-8): 45-47 és 2
(9) 7-10, 1995.
4. Fövényi J: Orális
antidiabeticumok 1997. Gyógyszereink 47: 153-160, 1997.
5. Cacciapuoti, F, Spiezia, R, Bianchi,
U, Lama, D, D’Avino, M, Varricchio, M: Effectiveness of glibenclamide on myocardial
ischemic ventricular arrhythmias in non-insulindependent diabetes mellitus. Am J Cardiol
67: 843-847, 1991.
6. Pogátsa G: Az orális
antidiabetikumok cardiovascularis hatásai. Diab Hung 5 (Suppl 2): 87-94, 1997.
7. Sonnenblick, M, Shilo, S:
Glibenclamide induced prolonged hypoglycemia. Age Ageing 15: 185-189, 1986.
8. Berger, W, Caduff, F, Pasquel, M,
Rump, A: The relatively frequent incidence of severe sulfonylurea-induced hypoglycemia in
the last 25 years in Switzerland. Results of 2 surveys in Switzerland in 1969 and 1984.
Schweiz Med Wochenschr 116: 145-151, 1986.
9. Jermendy Gy: Klinikai megfigyelések
orális antidiabeticum okozta súlyos hypoglykaemiás coma eseteiben. Medicus Universalis
10: 253-255, 1977.
10. Pogátsa G, Koltai M Zs: A
mikronizált és nem-mikronizált glibenclamid anyagcserehatásának összehasonlítása.
Diab Hung 6: 61-65, 1998.
11. Hantzschel, U, Wurlitzer, M,
Hanisch, R, Bothe, E, Dempe A: Treatment of newly diagnosed type II diabetic patients with
special reference to prescribing glibenclamide in low doses. Z Gesamte Inn Med 44:
137-143, 1989.
12. Arnqvist, HJ, Karlberg, BE,
Melander, A: Pharmacokinetics and effects of glibenclamide in two formulations, HB 419 and
HB 420, in type 2 diabetes. Ann Clin Res 15 (Suppl 37):21-25, 1983.
13. Scheen, AJ, Jaminet, C, Luyckx, AS,
Lefebvre, PJ: Pharmacokinetics and pharmacological properties of two galenical
preparations of glibenclamide, HB419 and HB420, in noninsulin-dependent (type 2) diabetes.
Int J Clin Pharmacol Ther Toxicol 25: 70-76, 1987.
14. Hoffman, A, Fischer, Y, Gilhar, D,
Raz, I: The effect of hyperglycaemia on the absorption of glibenclamide in patients with
non-insulin-dependent diabetes mellitus. Eur J Clin Pharmacol 47: 53-55, 1994.
15. Ikegami, H, Shima, K, Tanaka, A,
Tahara, Y, Hirota, M, Kumahara, Y: Interindividual variation in the absorption of
glibenclamide in man. Acta Endocrinol (Copenh) 111: 528-532, 1986.
16. Haupt, E, Putschky, F, Zoltobrocki,
M, Schoffling, K: Pharmacodynamics and pharmacokinetics of 2 glibenclamide preparations in
type 2 diabetes. Intraindividual double-blind comparison of Euglucon 5 (HB 419) and
Euglucon N (HB 420). Dtsch Med Wochenschr 109: 210-213, 1984.
17. Neugebauer, G, Betzien, G, Hrstka,
V, Kaufmann, B, Möllendorff, E von, Abshagen, U: Absolute bioavailability and
bioequivalence of glibenclamide (Semi-Euglucon N). Int J Clin Pharmacol Ther Toxicol 23:
453-460, 1985.
18. Carlson, RF, Isley, WL, Ogrinc, FG,
Klobucar, TR: Efficacy and safety of reformulated, micronized glyburide tablets in
patients with non-insulin-dependent diabetes mellitus: A multicenter, double-blind,
randomized trial. Clin Ther 15:
19. Halmos T, Kautzky L, Grósz A: A 2.
típusú cukorbetegség (NIDDM) kezelésének javallatai és elgondolkodtató
ellenjavallatai. Medicus Universalis 25: 21-23, 1992.
20. United Kingdom Prospective Diabetes
Study (UKPDS) 13: Relative efficacy of randomly allocated diet,
sulphonylurea, insulin, or metformin in patients with newly diagnosed noninsulin-dependent
diabetes followed for three years. Br Med J 310: 83-88, 1995.