Országos Korányi Tbc és Pulmonologiai Intézet, X.
Belgyógyászat
AZ ORGANIKUS SPONTÁN HYPOGLYKAEMIA
SZINDRÓMA DIAGNÓZISA 13 INSULINOMÁS ESET TÜKRÉBEN
Szilágyi Ruth dr., Halmos Tamás dr., Suba Ilona dr., Kautzky
László dr.
Összefoglalás
Az elmúlt
három évtizedben a szerzők 13 insulinomát kórisméztek. A betegek első csoportját
1968 és 1974 között, további 8 beteget 1980 és 1997 között észleltek. A szerzők
áttekintik az insulinoma diagnózisának eszköztárát, valamint a
differenciáldiagnosztika föbb elemeit. Valamennyi insulinoma soliter volt, malignitást
egy esetben sem észleltek. 13 betegünkböl az első csoportban két esetben történt
vakresectio. Preoperatíve 6 esetben tudtuk lokalizálni az insulinomát. Az 1980 után
diagnosztizált betegek közül egynél sem történt vakresectio, bár preoperatíve csak
4 esetben sikerült a lokalizáció. A másik négynél perioperatív ultrasonographia és
palpatio vezetett eredményhez. Az organikus hypoglykaemia diagnózisa eszméletvesztés,
extrém alacsony vércukorszint, magas endogén inzulinszint alapján nem nehéz. Az
insulinoma lokalizációja azonban még ma sem könnyű, gyakran csak műtét során
derül ki a tumor helye.
Kulcsszavak: spontán
hypoglykaemia, insulinoma
Diagnosis of
organic spontaneous hypoglycaemic syndrome based on the experiences of 13 insulinoma cases
Summary
The authors
diagnosed 13 insulinomas in the last 3 decades. The first group of patients (5 patients)
between 1968 and 1974, a second one between 1980 and 1997 (8 patients) was observed. The
aim of the present article was to evaluate the different diagnostic procedures in the
investigated periode. All insulinomas were soliter. None of them were malignant. In two
patients of the first group a „blind resection” had to be carried out (in one
repeatedly). In the second group blind resection could have been avoided, though the
preoperative localisation was only at four patients possible. At the remaining four
patients intraoperative sonography in combination with digital palpation could help the
correct localisation. Diagnosis of organic hyperinsulinism based on unconscious episodes
and corresponding high endogenous insulin levels is usually not difficult. Topographic
diagnosis however is still time-consuming and often problematic. In certain cases only
perioperative sonography and palpation casts light on the localisation of the tumor.
Key words: spontaneous
hypoglycaemia, insulinoma
Nem meglepő, hogy néhány évvel az
inzulin felfedezése után már leírták a hypoglykaemia tüneteit. A hypoglykaemia
fogalma sokáig tisztázatlan, illetve vitatott volt, mert mind az alkalmazott módszerek,
mind a vérvétel helye a vércukorértékeket jelentősen befolyásolják.
A hypoglykaemiával összefüggő tünetek
alapján a betegek két nagy csoportba oszthatók.1 A funkcionális hypoglykaemiás csoportba
azon betegek tartoznak, akiknek tüneteit döntöen az adrenerg, elhárító mechanizmus
magyarázza, vagyis itt a sympatoadrenalis rendszer hiperaktivitása (tachycardia,
remegés, verejtékezés, éhségérzés stb.) uralja a klinikai képet. Ezek a betegek
eszméletüket sohasem vesztik el, a viszonylag alacsony vércukorszintet az adrenerg
mechanizmus kompenzálja, a tünetcsoport inkább étkezést követően („fed state”)
alakul ki. Ezt a hypoglykaemia típust másként stimulatív hypoglykaemiának is nevezi
az irodalom, s abban megegyeznek a klinikusok, hogy ezen tünetek mögött inkább
neuropathiás személyiség, semmint valódi kórosan csökkent vércukorérték rejlik.
Az éhezési hypoglykaemia, helyesebben
neuroglycopenia a klinikai gyakorlatban „organikus” hypoglykaemiaként ismert.
Itt az adrenerg tünetekkel szemben az agyi struktúrák glukózhiánya dominál, s a
tünetegyüttes neuropsychiatriai tünetekben teljesedik ki, így a megváltozott
magatartástól a zavartságig, majd epileptiform convulsióig és comatosus állapotig
terjed. Ez utóbbit szokás „éhomi”, vagyis inkább hosszabb éhezési periódus
után (rendszerint hajnalban!) kialakuló („fasted state”) hypoglykaemiának nevezni.
Az ebbe a tünetcsoportba sorolható betegek organikusnak tünő neuropsychiatriai
tüneteket produkálnak, melyek előbbutóbb tudatvesztésbe torkollanak. Ez a súlyos
állapot intravénás cukor adására rendszerint gyorsan rendezhető.
A hypoglykaemiás állapotok ismert
amerikai kutatója, Service F.J. néhány éve egy újabb felosztást javasolt.2 Az első csoportban „egészségesnek
látszó” betegröl beszél, ahol a hypoglykaemia váratlanul, minden addig ismert ok
nélkül lép föl. Az insulinomákat ebbe a csoportba sorolja. A másik csoportba a már
eleve ismert krónikus betegség mellett fellépő hypoglykaemiás állapotok tartoznak,
pl. Addison-kór, anorexia nervosa, hypophysis-elégtelenség, nem béta-sejtes tumor. Ez
a felosztás egyelőre még nem ment át az orvosi köztudatba.
Az organikus hypoglykaemia alapvetően
két nagy csoportba osztható:
A
hyperinsulinaemiával járó esetekben a roszszullét tetöpontján rendszerint – az
alacsony vércukorértékekkel egyidőben – a serum inzulinszintje emelkedett,
A hyperinsulinaemiás hypoglykaemia
(neuroglycopenia) eredete a pancreas insulinomája, ritkábban diffúz hyperplasiája,
esetleg tubuloacinaris neoformáció (nesidioblastosis).3,4,5,6 A hyperinsulinaemia nélküli
organikus hypoglykaemiák létrejöhetnek bizonyos endokrin betegségek (Addison-kór stb)
következtében, de sokkal gyakrabban hypoglykaemisaló, extrapancreaticus tumorok állnak
a tünetek hátterében.
A régebbi biológiai
inzulinmeghatározások, melyek csak „inzulinszerű aktivitást” (ILA) mutattak ki,
gyakran extrém inzulinszint-emelkedésre utaltak, de a „valódi inzulin”
meghatározása során később kiderült, hogy a vércukorcsökkentő hatásért nem az
inzulin, hanem az extrapancreaticus tumor által szecernált növekedési faktor (IGF-2) a
felelős.7,8,9 Ez a tünetegyüttes az
“extrapancreaticus hypoglykaemisaló tumorok” gyűjtő elnevezést kapta s számos
alcsoportját írták már le.
Mi jelen közleményünkben a
hyperinsulinaemiával járó pancreas eredetű organikus formákkal foglalkozunk 13 saját
esetünk kapcsán.
A betegek első csoportját 1968 és 1974
között (5 beteg), a második csoportot (8 beteg) 1980 és 1997 között kórisméztük.
E dolgozat célja kettös: egyrészt
ismertetjük a diagnosztikus eszköztárat annak tükrében, hogy milyen eljárások a
legeredményesebbek, s menynyit fejlődött a diagnosztika az elmúlt évtizedek során,
másrészt néhány fontosabb differenciáldiagnosztikai szempontot tárgyalunk, melyek a
mindennapi klinikai gyakorlatban jelentősek.
Módszerek
A vércukorszintet standard laboratóriumi
módszerrel (GOD-POD-PAP) mértük. Korábbi években az ILA-t saját módszerünkkel
határoztuk meg.2 Éhgyomri értéke 100 µU/ml-ig
normális.
Az IRI-t RIA (I125) készlettel mértük (RK–12,
Izotóp Intézet). Éhgyomri értékének normális tartománya: 5–35 µU/ml.
A szérum C-peptid-szintjét RIA
módszerrel határoztuk meg (Serono), normális éhgyomri tartománya: 1–3 ng/ml.
Esetismertetések
1. K. M. 45 éves
férfi beteg. 1963 óta voltak elsősorban hajnalban jelentkező, convulsiókkal járó
eszméletvesztései. Ezen periódusok alatt vércukorértékei mérhetetlenül alacsonyak,
ILA-értékei pedig magasak – 700–3000 µU/ml – voltak.
Az IRI egy alkalommal volt magas (120
µU/ml). 4 év alatt 40 kg-ot hízott. Topográfiai vizsgálatai a következők voltak:
hypotoniás duodenographia, szelén-metionin scintigraphia, majd szelektív angiographia.
A pontos diagnózishoz a szelektív angiographia vezetett. műtét során a jelzett helyen
a pancreas farki részében kisdiónyi insulinomát találtak, melyet sikerrel
eltávolítottak.
2. V. I.-né, 41
éves. Anamnézisében éhezés során jelentkező görcsökkel járó eszméletvesztések
voltak. A rosszullétek alatti mérhetetlenül alacsony vércukorérték mellett az ILA:
1000 µU/ml, az IRI: 128 µU/ml volt. Topográfiai vizsgálatai: hypotoniás
duodenographia, szelén-metionin scintigraphia, retrográd pancreatographia, melyek
negatív eredményt adtak. Ezután vakresectio történt a farki részböl. Insulinoma nem
igazolódott, tünetei ismét jelentkeztek. Ismételt vakresectio során a resecatumban
ezúttal borsónyi insulinomát találtak. A beteg panaszmentessé vált.
3. W. L.-né, 57
éves. Convulsiókkal járó eszméletvesztéses hypoglykaemiák miatt kezdtük
vizsgálni. Rosszullétei során a vércukor 1,7 mmol/l, az ILA 3000 µU/ml, IRI 148
µU/ml volt. Topográfiai vizsgálatok: hypotoniás duodenographia, szelén-metionin
scintigraphia, ERCP, szelektív angiographia. A lokalizáció nem járt sikerrel. Négy
éven belül három resectiós műtétje volt, a harmadik resecatumban 3x7 mm nagyságú
insulinoma igazolódott. A beteg a posztoperatív szövődményekbe belehalt.
4. V. I.-né, 39
éves. 9 éven át epilepsiásként tartották nyilván convulsiókkal járó
eszméletvesztései miatt. Éhezéses eszméletvesztéskor vércukorszintje 1,3 mmol/l, az
IRI értéke 108 µU/ml volt. Topográfiai vizsgálatai: ERCP, szelén-metionin
scintigraphia, szelektív angiographia nem voltak eredményesek. Vakresectio történt
negatív eredménnyel. Diazoxidot kapott jó effektussal, majd tünetei három év múlva
ismét jelentkeztek. Ekkor hasi UH-vizsgálat a pancreas feji részében borsónyi
terimét mutatott, mely sebészi eltávolításakor insulinomának bizonyult.
5. W. S.-né
hypoglykaemiával járó eszméletvesztései 45 évesen kezdödtek. Tudatzavara során
mért vércukorértéke 2,3 mmol/l, IRI-értéke 88 µU/ml volt. Topográfiai
vizsgálatai: szelén-metionin scintigraphia, ERCP, szelektív angiographia negatívak
voltak. műtétbe nem egyezett bele, Diazoxidot kapott 7 éven át. 1979-ben került
műtétre, ekkor a sebész a pancreas feji részében tapintott borsónyi resistentiát,
melynek szövettani eredménye insulinoma volt.
6. S. M. nöbetegnek
26 éves korától voltak eszméletvesztéssel járó rosszullétei. Eszméletvesztése
alatt mért vércukorértéke 1,2 mmol/l, IRI-értéke 164 µU/ml volt. A topográfiai
vizsgálatok negatívak voltak. Diagnózis: perioperatív UH-vizsgálat a test és a farok
határán megtalálta a 6x8 mm nagyságú insulinomát, melyet sikeresen eltávolítottak.
7. SZ. M. 61 éves
férfi beteg tünetei hajnali convulsiókkal járó eszméletvesztések voltak.
Éheztetéssel tudatzavar volt provokálható, ekkor vércukra 2,3 mmol/l, IRI-értéke
108 µU/ml volt. Topográfiai vizsgálatai – hasi UH, hasi CT – negatívak voltak.
Diagnózis: a perioperatív UH-vizsgálat a pancreasfejben 4x7 mm nagyságú terimét
mutatott, amely a sikeres műtét során insulinomának bizonyult.
8. S. G. férfi
betegnek 43 éves korától voltak eszméletvesztéssel járó rosszullétei.
Éheztetéssel provokálva vércukra 2,3 mmol/l, IRI-értéke 78 µU/ml. Topográfiai
vizsgálatok: hasi UH, hasi CT negatív, endocopos Uhvizsgálat a fej és a test határán
észlelt 4x7 mm nagyságú elváltozást. Sikeres műtéte után a resecatum vizsgálata
insulinomát igazolt.
9. B. G. férfi
betegnek 39 éves korától voltak eszméletvesztéses rosszullétei. Epilepsiásként
kezelték. Éhezéssel provokálható volt, ilyenkor vércukorszintje 2,6 mmol/l,
IRI-értéke 76 µU/ml. A topográfiai vizsgálat – hasi UH – a pancreasfejben 4x8 mm
nagyságú terimét mutatott ki. A sikeres műtét insulinomát igazolt.
10. J. P.-nének 41
éves korában kezdödtek convulsióval járó eszméletvesztései. Éhezéssel
provokálva vércukra 2,8 mmol/l, IRI-értéke 102 µU/ml volt. Topográfiai vizsgálatok:
a hasi UH negatív volt, a hasi CT azonban a pancreasfejben 4x9 mm nagyságú terimét
észlelt, melyet a perioperatív UH-vizsgálat is igazolt. Sikeres műtétének
resecatumában insulinoma volt kimutatható.
11. U. A. férfi
beteg 25 éves korában, 1985-ben kezdödtek tudatzavarral járó rosszullétei. 12 órás
éhezés után vércukra 2 mmol/l alatt, IRI-értéke 46 µU/ml volt. Topográfiás
vizsgálatok: hasi UH, hasi CT, szelektív angiographia negatívak voltak. A műtét
során a pancreasfarokban tapintott, sikeresen eltávolított borsónyi képlet
szövettanilag insulinomának bizonyult.
12. J. Gy. férfi
betegnek 44 éves korától jelentkeztek eszméletvesztéses rosszullétei. 2 év alatt 12
kg-ot hízott. 14 órás éhezés után 2 mmol/l alatti vércukrot, 160 µU/ml IRI-t
mértünk. Topográfiai vizsgálatok közül a hasi UH és a CT negatív, az endoscopos
UH-vizsgálat a pancreas feje és teste határán észlelt 20 mm átmérőjű hypodens
képletet, mely a sikeres műtét során insulinomának bizonyult.

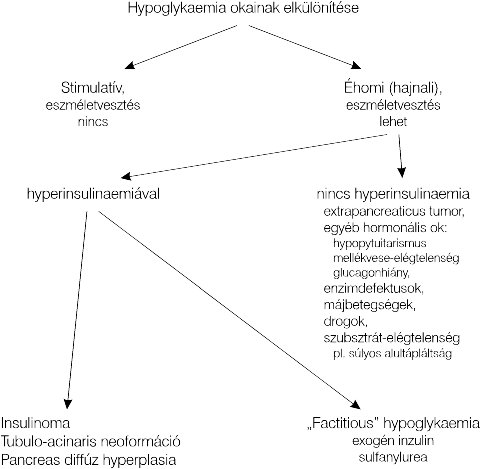
1. ábra: A feltételezett insulinomák kórismézése
Megbeszélés
A feltételezett insulinomák
kórismézése két szakaszban történik (1 ábra).
Az első szakaszban el kell
dönteni, hogy az eszméletvesztéssel járó neuroglycopeniás rosszullétek
hyperinsulinaemiával járnak-e vagy sem?
A második szakaszban a
feltételezett insulinoma lokalizációja történik.
1. A serum
mérsékelten emelkedett inzulinszintje pancreas eredetű, de nem feltétlenül insulinoma
okozta hyperinsulinismusra is utalhat. Ilyen pl. a tubulo-acinaris neoformáció (vagy
nesidioblastosis) és a diffúz insularis hyperplasia.3,4,5,6 Az ún. diffúz insularis hyperplasia
létezése nem bizonyított. A régebbi irodalomban speciális mikroszkópos számolási
eljárásokkal igyekeztek a Langerhans-szigeteket megszámolni, s bizonyos számú sziget
megszámolása és „normális mennyiségű Langerhans-struktúrával rendelkezö”
hasnyálmiriggyel történt összevetése alapján állították fel a
„sziget-hyperplasia” diagnózisát. Kérdéses, hogy ez a számolás mennyire volt
exakt, illetve, hogy ennek alapján mennyiben lehetett e kórkép felelős a kialakult
tünetekért?
Speciális kórkép a tubulo-acinaris
neoformáció, mely elsősorban újszülötteken, csecsemökön fordul elő, de
kivételesen felnőttkorban is kimutatható.3,4,5,6
Ilyenkor a pancreas exokrin funkciót
végző acinus sejtjei megörzik (vagy visszanyerik) eredeti „szigetépítö”
tulajdonságukat, vagyis kifejezett hyperinsulinaemiával járó tudatvesztéses
állapotok alakulhatnak ki. A kép nagyon nehezen különíthető el az insulinomától.
Az elkülönítő diagnózis elemei: tudatvesztéses állapotban itt extrém alacsony
vércukorszint mellett a serum inzulin- és C-peptid-értékei általában csak
mérsékelten emelkedettek, sosem érik el az extrém magas értéket. Képalkotó
eljárásokkal körülírt elváltozást sosem lehet detektálni.11 Feltételezhető, de erre irodalmi
adatot nem találtunk, hogy a proinzulin/inzulin arány nagyobb a megszokottnál, hiszen a
kevésbé érett béta-sejtek feltételezhetöen több proinzulint termelnek, mint
normális körülmények között. (Az NIDDM kezdeti periódusában ez az arány szintén
magasabb!) Végső soron ez a diagnózis kizárásos alapon állítható fel, exakt módon
csak a pancreasszövettan bizonyíthatja. Ilyen esetekben gyakran kerül sor ún.
vakresectio elvégzésére, itt a resecatum szövettani vizsgálata vezethet eredményre. Esetismertetés: K. J.-nét 71
éves korában nyolc éve fennálló éhezési hypoglykaemiás panaszokkal kezdtünk
vizsgálni. Endogén inzulinértékei nem voltak magasak. A pancreasban insulinomát
lokalizálni nem sikerült. Hypoglykaemiával járó eszméletvesztései miatt Diazoxid
kezelésben részesült, majd ennek eredménytelensége miatt Streptozotocin kezelést
kapott az art. coeliacába. A kezelések ellenére hypoglykaemiás eszméletvesztései
továbbra is voltak. Végül a beteget veseelégtelenség miatt elvesztettük. Sectio
során a diagnózis nesidioblastosis volt.
2. Exogén
hyperinsulinismusok: a hyperinsulinaemiával járó eszméletvesztés hátterében
„müvi” (factitious) beavatkozás is állhat, pl. a beteg nagy mennyiségű exogén
inzulint kapott (öngyilkosság), vagy nagy adagban vett be sulfanylureákat.12 Inzulinnal történt gyilkosságokról
is beszámoltak néhány esetben. A diagnózis elvei a bármilyen indítékból történö
inzulin túladagolással egyeznek meg.13
Az endogén és az exogén
hyperinsulinaemia elkülönítésében a C-peptid- és a proinzulinszint mérése nyújt
segítséget.1 Exogén inzulin túladagoláskor a
serum inzulinszintje magas, de a Cpeptid értéke inkább alacsonyabb az exogén inzulin
szupprimáló hatása miatt.
A sulfanylurea túladagolását elsősorban
a paramedikális személyzethez tartozók között írták le. A diagnózishoz a
sulfanylurea vérböl és/vagy vizeletböl való kimutatása vezet. Hasonló
indíttatásból, mint az inzulin túladagolás esetén, ezen egyének is kórházba
kívánnak kerülni, s vállalják az esetleges műtétet is (Münchhausen-szindróma).
Esetismertetés: az
59 éves sovány nöbeteg anamnézisében több eszméletvesztéses rosszullét szerepelt.
Egy ízben ilyenkor 1 mmol/l alatt volt a vércukra. Insulinoma gyanújával vettük fel.
Az éheztetéses próba 16 óra után pozitív volt, extrém alacsony vércukorszint
mellett a beteg eszméletlenné vált. Serumának inzulinszintje ekkor 64 µU/ml volt,
C-peptid-szintet ekkor még nem volt lehetőségünk mérni. Minden képalkotó eljárás
negatív volt. Eszméletvesztései másodnaponta ismétlődtek. Már resectiós műtétet
terveztünk, amikor szekrényében több száz glibenclamid tablettát találtunk (a beteg
nem volt cukorbeteg). Szembesítve a felfedezéssel, a beteg magyarázat nélkül azonnal
távozott.
Az insulinoma diagnózisának második
szakasza általában sokkal nehezebb, mert bár a kórismét valószínűsítettük,
de a tumor lokalizációja hiányzik.14,15,16,17 Betegeink első csoportjában a
kórisme eszközei még kevésbé voltak hatékonyak.
Az első öt beteg közül egy betegnél a
szelektív angiographia vezetett eredményre, egy másik betegben az ekkor még korántsem
ennyire fejlett hasi ultrahang vizsgálat találta meg a borsónyi nagyságú tumort, míg
a harmadik betegünkben csak a perioperatív sebészi tapintás vezetett eredményre. Két
betegben ismételt resectiós műtét történt (vakresectio).
Betegeink második csoportjában 3
betegnél a perioperatív UH-, 2 esetben az endoscopos UHvizsgálat, 18,19 egy további esetben a hasi CT, és
egy másik esetben a hasi UH mutatta meg az insulinoma helyét a pancreasban. 2 esetben a
perioperatív palpatio vezetett eredményre. A topogáfiai vizsgálatok a második
csoportban (8 beteg) tehát eredményesebbek voltak, ún. vakresectiót egy esetben sem
kellett végezni (1. táblázat).
| 1974 előtt: (esetszám 5 beteg) | ||
| összes | diagnosztikus | |
| vizsgálatszám | ||
hypotoniás |
3 | 0 |
szelén-metionin |
5 | 0 |
retrográd |
4 | 0 |
szelektív angiographia |
4 | 1 |
hasi UH |
1 | 1 |
perioperatív palpatio |
(5) | 1 |
(vakresectio) |
3 | 2 |
1980 után: (esetszám 8 beteg) |
||
| összes | diagnosztikus | |
| vizsgálatszám | ||
szelektív angiographia |
2 | 0 |
hasi UH |
8 | 1 |
hasi CT |
6 | 1 |
endoscopos UH |
3 | 2 |
szomatosztatin- |
1 | 0 |
pancreas-MR |
0 | |
perioperatív UH |
3 | 2 |
perioperatív palpatio |
(8) | 2 |
(vakresectio) |
0 | 0 |
1. táblázat: Topográfiai
vizsgálatok insulinoma lokalizálásához
Az irodalomban értékesnek mondott
MRvizsgálatot20 és az újabban javasolt
intraarterialis kalcium-glukonát hatását az insulinoma preoperatív lokalizációjában21 egyik betegünknél sem állt
módunkban kipróbálni. A szomatosztatinreceptor scintigraphiás (octreoscan)
vizsgálatot egy esetben végeztük el, eredménytelenül.22
IRODALOM
1. Lehman, R,
Spinas, GA: Abklarung von Hypoglykämien. Schweiz Med Wochenschr 124: 1155-61, 1994.
2. Service, FJ: Hypoglycemic
disorders. N Engl J M 332: 1144-1150, 1995.
3. Halmos T,
Korányi L, Salamon F, Szücs L, Tarjányi M: Die Wirkung des Streptozotocins auf das
bei chronischen Pankreatitis durch Neoformation der langerhansschen Inseln entsandene
organische hypoglycaemie Syndrom. Endokrinologie 65: 354-59,1975.
4 Farley, DR, van
Heerden, JA: Adult pancreatic nesidioblastosis. Arch Surg 129: 329-332, 1994.
5. Walmsley, D,
Matheson, NA: Nesidioblastosis in an elderly patient. Diabet Med 12: 542-545, 1995.
6. Garcia, JP,
Franca, T, Pedroso, C: Nesidioblastosis in the adult surgical management. HPB Surg 10:
201-209, 1997.
7. Perros, P,
Simson, J: Non islet cell tumor-associated hypoglycaemia. Clin Endocrinol 44:
727-731,1996
8. Kuenen, BC,
van Doorn, J: Non- islet -cell tumour induced hypoglycaemia. Neth J Med 48 :175-9,
1996.
9. Hoog, A,
Sandberg, NAC, Hulting, AL: High-molecular weight IGF-2 expression in a
haemangiopericytoma associated with hypoglycaemia. APMIS 105: 469-482, 1997.
10. Halmos T,
Salamon F, Loczka B: Ein neues biologisches verfahren zur insulin bestimmung. Aerztl
Forsch 17: 467-60, 1963.
11. Halmos T: A
felnőttkori spontán hypoglycaemiás tünetegyüttes. Budapest, Medicina, 1977.
12. Jermendy Gy: Hypoglykaemia
factitia – Münchhausensyndroma diabetes mellitusban. Orvosi Hetilap 136: 31-33, 1995.
13. Marks V: Hypoglycaemia
– Real and Unreal,lawful and unlawful: The 1994 Banting Lecture. Diabetic Med 12:
850-864, 1995.
14. Pedrazolli,
S, Pasquali, C: Surgical treatment of insulinoma. Br J Surg 81: 672-676, 1994.
15. Kisker, O,
Bastian, D: Diagnostic localisation of insulinoma. Experiences with 25 patients. Med
Klin 91:349-54, 1996.
16. Grant, CS: Gastrointestinal
endocrine tumours. Insulinoma. Baillieres Clin Gastroenterol 10: 645-671, 1996.
17. Bliss, RD,
Carter, PB, Lennard, TW: Insulinoma: a review of current management. Surg Oncol 6:
49-59, 1997.
18 Pitre, J,
Soubrane, O: Endoscopic ultrasonography for the preoperative localization of
insulinoma. Pancreas 13: 55-60, 1996.
19. Thompson, NW,
Czako, PF: Role of endoscopic ultrasonography in the localization of insulinomas and
gastrinomas. Surgery 116: 1131-8, 1994.
20. Pavone, P,
Catalano, C: Identification of pancreatic insulinomas. The role of magnetic resonance.
Radiol Med 90: 734-9, 1995.
21. Defreyne, L,
König, K, Lerch, MM: Modified intra-arterial calcium stimulation with venous sampling
test for preoperative localization of insulinomas. Abdom Imaging 23: 322-331, 1998.
22. Breeman, WAP,
van Hagen, PM: Somatostatin receptor scintigraphy using /11In-DTP A0/RC-160 in humans:
a comparison with /11In-DTPA0/ octreotide. Eur J Nucl Med 25: 182-186, 1998.